|
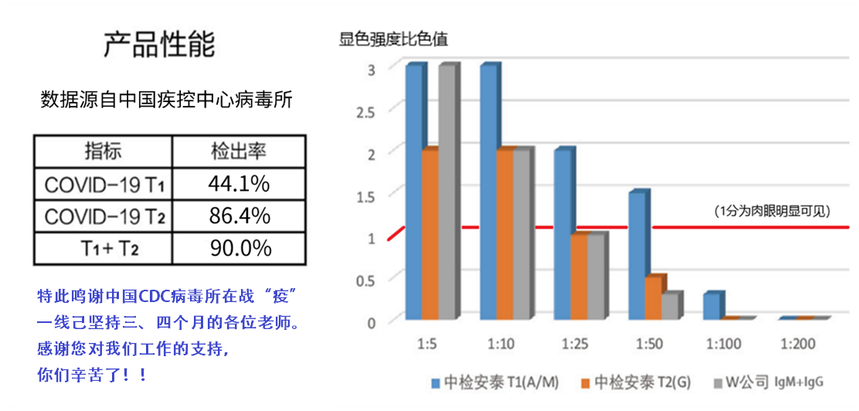
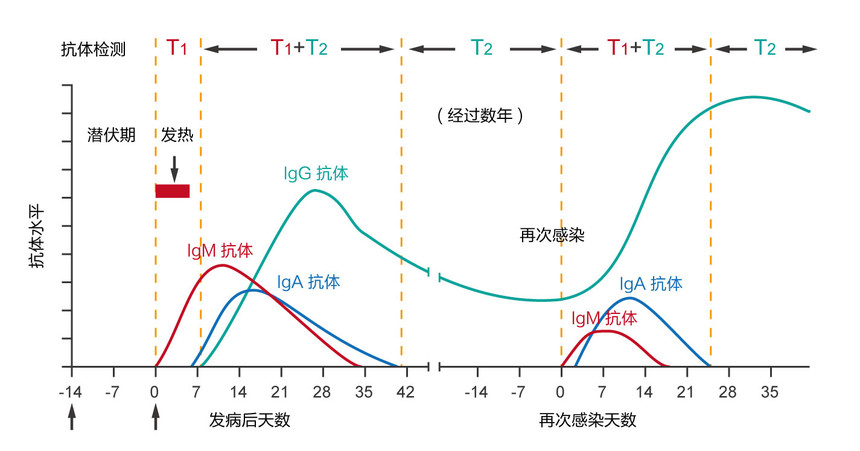
全球首家!中检安泰独家产品新冠病毒IgA/IgM/IgG抗体联合检测崭露头角!时间:2020-03-25 点击蓝字,关注我们 全球首家 新冠病毒IgA/IgM/IgG抗体联检 (中国检验安全 责任重于泰山) 在2020年春节期间新型冠状病毒疫情爆发后,以“一场抗击新冠病毒感染的肺炎疫情阻击战在全国骤然打响”的方式拉开序幕。目前,新型冠状病毒感染已肆虐全球,全球新冠病毒感染人数与日俱增。 当前,国内外免疫方法的新型冠状病毒诊断产品主要是总抗体以及IgM、IgG抗体联合检测试剂,而新型冠状病毒特异性IgA抗体检测属于空缺状态。全球首创可检测COVID-19特异性IgA抗体产品现已面世。北京中检安泰诊断科技有限公司新上市的“新型冠状病毒(COVID-19)IgA/IgM/IgG抗体联合检测试剂盒(胶体金法)”可对新冠病毒(COVID-19)特异性IgM、IgA、IgG抗体进行联合检测,而且使用新冠病毒S1蛋白与S2蛋白进行标记,采用冻干工艺确保产品具有高灵敏度和特异性,填补了新冠病毒快速免疫诊断多项抗体联合检测的空白市场。 目前该试剂盒已获得欧盟CE准入资格,作为全球首家研发出新冠病毒IgA/IgM/IgG抗体联合检测的厂家,中检安泰具有10年层析技术研发经验,ISO13485体系认证,产品工艺稳定可靠,将为全球疫情阻击战、为临床精准检测提供最新武器。 北京中检安泰诊断科技有限公司于2020年1月就开始攻关研发新型冠状病毒检测试剂,截止至2020年2月新型冠状病毒(COVID-19)lgA/IgM/IgG抗体联合检测试剂盒(胶体金法)在科研人员夜以继日的努力下完成了研发工作,现评估产品灵敏度和特异性已经达到一个满意的结果,开始进行有效的产能转化放大生产工作。COVID-19 lgA/IgM/IgG抗体联合检测试剂在患者的急性感染期以及恢复期均可用于检定,能与对感染早期高敏感性的核酸检测试剂形成有效互补,且无需仪器直接判读。 在武汉市,由中国疾控中心病毒所使用59例的临床确诊患者样本进行评估后的反馈结果看,中检安泰生产的新型冠状病毒(COVID-19)IgA/IgM/IgG抗体联合检测试剂盒阳性检出率达到了90%;公司研发实验室采用疫情爆发之前采集的随机样本检测,试剂特异性为94.5%。 使用中检安泰诊断科技有限公司生产的新型冠状病毒(COVID-19)IgA/IgM/IgG抗体联合检测试剂对比某已上市的W公司的新型冠状病毒抗体检测试剂;检测同一新型冠状病毒感染患者样本,并进行梯度稀释验证,比对两产品灵敏度水平差异。 通过比对,确认中检安泰诊断科技有限公司产品灵敏度要高于已上市W公司产品灵敏度水平。满足临床使用中对已感染或疑似患者的辅助筛查。 01 产品优势 1. 全球首家,IgA+IgM+IgG抗体联合检测,可有效诊断早期及现症感染,并区分既往感染; 2. 高敏感性,检测IgA抗体,相比同方法学试剂,可提高阳性检出率。 3. 样本类型多样,全血、血清或血浆都可,无需前期处理; 4. 单人份独立包装,无需任何仪器设备,检测时间短,适合现场筛查; 5. 试剂盒常温储存,无需冷藏及冷链运输。 02 指标意义 IgA/IgM/IgG抗体联合快速检测可用于疾病病程发展的评估。T1指IgA和(或)IgM的检测结果,阳性结果提示可能为新近发生感染,可用于辅助诊断COVID-19的早期及现症感染;T2是IgG检测的结果,单独IgG阳性结果提示可能发生感染有一段时间,可用于辅助诊断COVID-19的中后期或既往感染。 新冠病毒IgA、IgM抗体检测可以很好的补充核酸阴性新冠感染患者的诊断,同时对于无症状感染患者的诊断也表现出较好的价值;聚焦早期诊断,尽可能缩小窗口期,对疑似病例的早诊断具有重要研究价值。 03 商务合作 该试剂现已被发往韩国,土耳其,伊拉克,伊朗、印尼、巴基斯坦、菲律宾、德国等多个国家。中检安泰作为全球医疗行业的一份子,砥砺奋进,愿为全球防疫做出应有贡献。 欢迎您的垂询! 网址:www.bjzjat.com 中检安泰上市全球独家产品新冠IgA/IgM/IgG抗体联合检测试剂盒的消息经过体外诊断网和CACLP体外诊断资讯等多家报道,阅读量和转载量到数万人次,引发众多关注。详情请点击链接: 北京中检安泰诊断科技有限公司成立于2010年,隶属于华卫天和集团旗下,立足于体外诊断试剂(IVD)研发、注册、生产与销售。针对免疫诊断市场和POCT市场,力求拓展体外诊断产品在医疗行业的新应用与普及。为广大医疗工作者辅助判断病患需要何种医疗方法及辅助指导治疗用药,提供必要的医学检验检测产品。公司产品的研发与规划具有明确的方向,产品具有操作简便、结果直观、省时省力、经济实惠的必备特征。产品研发过程中,大力挖掘产品固有优势以满足POCT市场与免疫诊断市场相关的旺盛需求。保持产品固有性能的优异及公司在行业内的技术优势。 |